Nietrzymanie stolca
1 III Katedra i Klinika Chirurgii Ogólnej Uniwersytetu Jagiellońskiego Collegium Medicum w Krakowie
2 Oddział Chirurgii Ogólnej Szpitala Miejskiego Specjalistycznego im. G. Narutowicza w Krakowie
Skróty: BF – trening behawioralny, biofeedback; ES – elektrostymulacja; FISI – skala Rockwooda; IFFGD – International Foundation of Functional Gastrointestinal and Motility Disorders; KSNS – krańcowe stadium nietrzymania stolca; MR – obrazowanie techniką rezonansu magnetycznego; NS – nietrzymanie stolca; TAUS – przezodbytowa ultrasonografia; USG – ultrasonografia
Wprowadzenie
Jedną z podstawowych czynności fizjologicznych wpływających na funkcjonowanie organizmu jest wydalanie, akt kontrolowany przez złożony układ nerwowo-hormonalny, którego efektorem jest mechanizm zaporowy – kompleks mięśni zwieraczy odbytu. Układ ten umożliwia podjęcie aktu defekacji w odpowiednim czasie i miejscu. Efektem upośledzenia czynności kompleksu zwieraczy odbytu jest objawowe nietrzymanie stolca (NS; faecal incontinence), czyli nabyta lub wrodzona utrata kontroli oddawania stolca. Jest to kalectwo eliminujące chorego z życia społecznego, dyskryminujące jego pozycję w rodzinie, a w skrajnych przypadkach może prowadzić do prób samobójczych.
Na podstawie badań przeprowadzonych w latach 1998–2000 częstość NS ocenia się na około 3–5% dorosłej populacji USA i Europy. Są to najprawdopodobniej jednak dane niedoszacowane, co wynikało wówczas z braku ujednoliconego nazewnictwa stosowanego do 2000 roku.1,2 Jednolita, zrozumiała i powszechnie uznana definicja NS to efekt pracy kilku referencyjnych ośrodków z Europy i USA, których doświadczenia pozwoliły na przyjęcie ogólnie akceptowanego nazewnictwa oraz algorytmów diagnostyczno-terapeutycznych, choć także one podlegają ciągłym modyfikacjom.3
Definicja nietrzymania stolca
Pod pojęciem NS powszechnie rozumie się objawy wynikłe z niewydolności mechanizmu zaporowego końcowego odcinka jelita grubego, jakim jest kompleks zwieraczy odbytu, przy czym dotyczą one zarówno stolca jak i gazów. Niewydolność owego mechanizmu nie zawsze wynika z morfologicznego ubytku zwieraczy. Może być następstwem ich odnerwienia (obwodowego lub ośrodkowego), a także zaburzeń odbioru bodźców czuciowych z kanału odbytu. W tym miejscu warto nadmienić, że niewydolność zwieraczy jako takich (anatomiczna lub czynnościowa) w języku angielskim nosi nazwę anal incontinence (nietrzymanie odbytowe), co jest pojęciem węższym od faecal incontinence, przy czym wyodrębniono skrajną formę upośledzenia funkcji zwieraczowych określaną mianem krańcowego stadium NS (KSNS) (end-stage faecal incontinence), która wymaga zaawansowanych procedur operacyjnych.3
Jak zobiektywizować czasami subiektywne objawy
Chorzy w zróżnicowany sposób określają subiektywne objawy NS, stąd trudności w interpretacji ich opisów. W celu ujednolicenia oceny objawów NS i ich nasilenia stosuje się skale: Rockwooda (fecal incontinence severity index – FISI), Jorge Wexnera (skala Cleveland), Veizeya, Pescatoriego, American Medical System Scale (fecal incontinence scoring system) czy też Holschneidera, uwzględniającą parametry manometrii odbytowej (Holschneider scoring scale, Holschneider AM Elektromanometrie des Enddarms). Nie stwierdzono natomiast znamiennych różnic pod względem efektywności oceny stopnia NS w zależności od liczby branych pod uwagę czynników.4 Zgodnie z zaleceniami International Conference on Fecal Incontinence we włoskim Bari zaleca się stosowanie FISI5 lub skali Jorge Wexnera6.
Patogeneza niewydolności funkcji zwieraczowych i objawowego nietrzymania stolca
Patomechanizm utraty kontroli nad aktem defekacji może być różnorodny. Zaburzenia mogą dotyczyć odbytu, odbytnicy lub ich wzajemnych relacji, czyli odruchów odbytniczo-odbytowych odpowiedzialnych za koordynację reakcji zwieraczy i odbytnicy. Zatem schematycznie mechanizm NS można przedstawić następująco:6,7
Biorąc pod uwagę powyższe, istnieją pewne określone sytuacje kliniczne sprzyjające występowaniu objawowej dysfunkcji zwieraczy opisane poniżej.
Nienowotworowe choroby jelit
Przewlekłe stany zapalne jelit (inflammatory bowel disease): wrzodziejące zapalenie jelita grubego, a zwłaszcza choroba Crohna, która w 10–30% przebiega z objawami anorektalnymi, mogą prowadzić do objawów NS u ponad 20% chorych, a nasilenie NS pozostaje w bezpośredniej korelacji z okresami zaostrzenia choroby. Czynnościowe choroby jelit z towarzyszącymi zaburzeniami motoryki jelita grubego. jak na przykład zespół jelita nadwrażliwego (irritable bowel syndrome) także generują 20% ryzyko NS.8 Również przewlekłe zaparcia mogą przebiegać z objawami NS; gdy masy stolca ulegają bakteryjnemu rozkładowi, dochodzi do niekontrolowanego wycieku płynnej treści (overflow incontinence).2
Chorzy po wycięciu odbytnicy z powodu nowotworu
Zwiększająca się z roku na rok zapadalność na raka odbytnicy oraz zastosowanie szwów mechanicznych i nowych technik operacyjnych zwiększyło znacznie liczbę chorych po zabiegach resekcyjnych z zachowaniem zwieraczy. Ryzyko wystąpienia objawów NS po takich zabiegach, zwłaszcza niskiej resekcji odbytnicy, wynosi 15–60% w zależności od wysokości zespolenia.9 Radioterapia przed- lub pooperacyjna znamiennie wpływa na funkcje anorektalne. Jest to wynikiem nie tylko odczynu zapalnego, ale także trwałych zmian histologicznych. Dochodzi bowiem do zniszczenia splotów śródściennych odpowiedzialnych za odruchy anorektalne.
Chorzy po zabiegach proktologicznych
Zabiegi takie jak wycięcie hemoroidów, wycięcie przetoki czy szczeliny z chirurgicznym przecięciem zwieracza wewnętrznego są obarczone ryzykiem wystąpienia objawów NS u 10–30% chorych w zależności od rodzaju zabiegu i doświadczenia operatora.
Okołoporodowe uszkodzenie zwieraczy
Objawy NS występują częściej u kobiet. Jest to związane z inną budową miednicy, krótszym kanałem odbytu, wpływem hormonów i przebytymi porodami.10 Szczególnie akcja porodowa z wydłużoną II fazą, powikłana pęknięciem krocza lub źle wykonanym jego nacięciem, a także zastosowanie kleszczy pociągają za sobą duże ryzyko poporodowego uszkodzenia zwieraczy, w tym także KSNS.11 Również poród prawidłowy u około 30% kobiet może wywołać różnego stopnia objawy NS. Przykładowo, częstość NS w grupie 20 500 rodzących w USA, u których doszło do pęknięcia krocza III i IV stopnia (5%), oceniono na ponad 40%. Dla porównania, u rodzących bez nacięcia krocza i bez powikłań ryzyko wystąpienia poporodowego NS wynosi około 1%. Podobne dane pochodzą z Niemiec, Anglii i Skandynawii. Nie ma jednoznacznych danych co do wpływu histerektomii, jednak zabieg ten przebyło ponad 50% kobiet z NS.2
Neurologiczne i układowe przyczyny zaburzeń kontroli defekacji
Rozwijająca się w przebiegu długoletniej cukrzycy polineuropatia u 20% chorych przebiega z objawami nietrzymania zarówno stolca jak i moczu.7 U około 25% osób cierpiących z powodu rwy kulszowej występują zaburzenia kontroli oddawania moczu i stolca. Według danych International Foundation of Functional Gastrointestinal and Motility Disorders (IFFGD) z 2002 roku 70% chorych po zabiegach neurochirurgicznych nie potrafi w pełni kontrolować wydalania stolca lub moczu.3 Stwardnienie rozsiane w ponad 50% przypadków przebiega z zaburzeniem kontroli defekacji.12 Ryzyko wystąpienia NS towarzyszy 80% chorych z rozszczepem rdzenia kręgowego oraz dotyczy 25–75% ofiar urazów rdzenia.3
Diagnostyka nietrzymania stolca
Badanie kliniczne
Brak lub zaburzenia jednego z wymienionych elementów odpowiedzialnych za kontrolę defekacji lub kombinacja kilku z nich prowadzi do wystąpienia objawów NS. Uzyskane w trakcie szczegółowego badania podmiotowego dane systematyzowane są na podstawie dzienników objawów i stanowią podstawę do wstępnej klasyfikacji NS z użyciem jednej z zalecanych, wymienionych wcześniej skal. W celu wykluczenia zmian organicznych chorych zawsze poddaje się badaniom diagnostycznym, takim jak ultrasonografia (USG), kolonoskopia, rektoskopia.13
Badania czynnościowe – manometria anorektalna
Manometrię anorektalną wykonuje się za pomocą różnych urządzeń: od przepływowych perfundowanych wodą, poprzez mikrobalonowe, na manometrach typu solid state probe wysokiej rozdzielczości kończąc. Badanie manometryczne ocenia następujące funkcje anorektalne:
– odruchowy skurcz zwieraczy w trakcie wzrostu ciśnienia tłoczni brzusznej (recto-anal reflex)
– relaksacja kompleksu zwieraczy w trakcie parcia na stolec (recto-anal inhibitory reflex).
Brak odruchów odbytniczo-odbytowych świadczy o przerwaniu przewodnictwa pomiędzy odcinkiem przedzwieraczowym i zwieraczami (np. w przypadku polineuropatii cukrzycowej). Ponadto badanie cewnikiem wielokanałowym umożliwia ocenę funkcji vector volume, czyli trójwymiarowego profilu ciśnień, odsetka radialnej asymetrii, a także czynnościowej długości strefy zwieracza (tj. strefy podwyższonego i maksymalnego ciśnienia). Z wykresu ciśnienia podstawowego i wspomaganego można wyliczyć wskaźnik zmęczenia zwieraczy (fatigue index), który lepiej ilustruje ich stan czynnościowy.
Wymienione badania manometryczne uważa się obecnie za standard w ocenie czynnościowych zaburzeń anorektum.14,15
Badania wizualizacyjne
Ultrasonografia przezodbytowa
Przezodbytowa USG (transanal ultrasonography – TAUS).
Badanie wykonuje się przy zastosowaniu specjalnych sond endorektalnych
(z wirującą głowicą) o zakresie częstotliwości minimum 7 MHz. Wynik TAUS
ma decydujący wpływ na wybór postępowania. Ubytek morfologiczny zwieraczy
przekraczający 1/3 ich obwodu zwykle wyklucza opcję leczenia zachowawczego.5,15
Obrazowanie techniką rezonansu magnetycznego
Obrazowanie techniką rezonansu magnetycznego (magnetic resonanse – MR),
zwłaszcza z zastosowaniem sondy doodbytniczej (coil MR) pozwala
precyzyjnie ocenić stan morfologiczny i czynnościowy zwieraczy (kurczliwość),
umożliwia także ich komputerową trójwymiarową wizualną rekonstrukcję.
Defekografia (wideoproktografia)
Defekografia jest rodzajem badania radiologicznego umożliwiającym
obrazowanie i analizę aktu defekacji. Tak zwana proktodefekografia to dynamiczne
badanie odbytnicy (dynamic rectal examination), a coraz powszechniej stosowana
obecnie wideoproktografia to badanie proktodefekograficzne z zapisem wideo.15
Oceniane są następujące parametry:
Badania elektrofizjologiczne
Test latencji nerwu sromowego
W teorii badanie latencji nerwu sromowego ma diagnozować zmiany patologiczne w obrębie włókien
nerwowych łączących efektor (zwieracze) z ośrodkowym układem nerwowym.
Wymaga specjalnego zestawu elektrod złożonego z elektrody stymulującej i rejestrującej oraz
wystarczająco czułej aparatury. W praktyce jednak
dopiero niemal całkowita demielinizacja lub innego typu uszkodzenie zaowocuje
znamiennym wydłużeniem czasu pomiędzy stymulacją i rejestracją. W literaturze
przedmiotu za najważniejszą uważa się publikację Hilla, przygotowaną na podstawie
wyników leczenia 2067 pacjentów. Nawet w oparciu o tak dużą liczbę przypadków
autorom doniesienia nie udało się wykazać użyteczności rzeczonego testu w diagnostyce NS.14 Obecnie
więc badanie to uważa się
za nieprzydatne w praktyce proktologicznej.
Elektromiografia igłowa
Elektromiografia igłowa ma na celu określenie ogólnej aktywności
mioelektrycznej zwieracza zewnętrznego i mięśnia łonowo-odbytniczego podczas spoczynku,
dowolnego skurczu zwieracza i aktu parcia na stolec.
Stosowane metody pomiaru (w tym przypadku koncentryczne elektrody igłowe)
pozwalają na jednoczesną ocenę aktywności kilku jednostek motorycznych.
Zgodnie z zaleceniami IFFGD elektromiografia igłowa, ze względu na niemiłe
odczucia w trakcie badania, jest wskazana, tylko gdy podejrzewa się
uszkodzenie unerwienia zwieracza zewnętrznego, w celu wykluczenia
ubytku w zakresie unerwienia obwodowego zwieracza.15
Elektromiografia powierzchniowa
Elektromiografia powierzchniowa polega na wykonaniu przezodbytowego
badania elektromiograficznego przy użyciu specjalnej wielokanałowej sondy.
Badanie jest nieinwazyjne i w odróżnieniu od elektromiografii igłowej
nie powoduje u pacjenta nieprzyjemnych wrażeń. Wielokanałowa sonda umożliwia
jednoczasową ocenę wielu jednostek motorycznych, a specjalne oprogramowanie
– dekompozycję sygnału i analizę czynności elektrycznej wraz z precyzyjnym
zlokalizowaniem stref unerwienia (lub ich nieobecności w przypadku uszkodzenia
gałęzi nerwu sromowego). Obecnie jednak badanie to jest dostępne tylko w nielicznych ośrodkach
europejskich (także w Pracowni Badań Czynnościowych
III Katedry Chirurgii Ogólnej UJ CM w Krakowie). Wymaga skomplikowanej i drogiej aparatury i odpowiednio
przeszkolonego personelu,
jednak aktualnie jest jedynym nieinwazyjnym badaniem
pozwalającym tak precyzyjnie diagnozować NS o etiologii neurogennej.
Ocena podatności i elastyczności ściany odbytnicy
Celem badań czucia trzewnego (wisceralnego) jest ocena napięcia ściany
jelita (tonus lub elastyczność), wyznaczenie progów czucia trzewnego,
oraz obliczenie podatności (compliance) badanego odcinka jelita
(np. odbytnicy lub okrężnicy).15
Badanie konieczne w każdym przypadku nietrzymania i zaparć,
szczególnie w zaburzeniach funkcji rezerwuarowej odbytnicy.
Inne badania diagnostyczne
Inne, rzadziej stosowane badania diagnostyczne obejmują między
innymi centralną lub obwodową stymulację magnetyczną czy też dynamiczną
defekografię z użyciem MR, są jednak stosowane w nielicznych ośrodkach i w celach głównie
naukowych.
Zachowawcze metody leczenia nietrzymania stolca
Postępowanie lecznicze zależy od przyczyny i stopnia NS. Z kolei wyniki leczenia zależą w dużej mierze od prawidłowej kwalifikacji, doboru metody leczenia oraz jego realizacji. W oparciu o kilkuletnie doświadczenie własne oraz wytyczne opracowane w wyniku współpracy pomiędzy ośrodkami w Europie i USA sformułowano ramowe algorytmy postępowania. Zasadą jest wykorzystanie wszystkich możliwych zachowawczych metod leczenia, zanim zapadnie decyzja o leczeniu operacyjnym. Nie dotyczy to wczesnej (<24 h) plastyki zwieraczy uszkodzonych w trakcie porodu.3
Do najprostszych zachowawczych metod leczenia NS należą:
Metody te skutecznie redukują objawy NS u około 20% chorych. Pozostała grupa wymaga działań bardziej inwazyjnych.
Trening behawioralny
Chorzy, u których nie wykryto defektu zwieraczy lub ich ubytek nie przekracza ¼ obwodu, przy zachowanym obwodowym unerwieniu, kwalifikują się do leczenia metodą treningu behawioralnego, popularnie zwaną biofeedback (BF).17,18
Biofeedback jest formą warunkowania instrumentalnego, „uczenia przez wzmocnienie”. Chory – obserwując wykres na monitorze – kontroluje poprawność wykonanego ćwiczenia (skurczu zwieraczy). Obecnie stosuje się aparaty oparte o rejestrację zapisu elektromiograficznego – elektroda umieszczona w kanale odbytu rejestruje aktywność elektryczną kompleksu zwieraczy odbytu podczas skurczu. O jego sile i poprawności świadczy liczba i kolor zapalanych diod świetlnych lub głośność towarzyszącego temu sygnału akustycznego. Ćwiczenia te powtarzane kilka razy dziennie (2–4 razy przez 15 minut) w różnych ułożeniach ciała po upływie kilku miesięcy powodują zwiększenie siły skurczu dowolnego oraz podstawowego napięcia kompleksu zwieraczy odbytu. Pacjenta zachęca się do wykonywania ćwiczeń w warunkach domowych. Skuteczność tej metody wynosi 50–80% (w zależności od źródła).17,19
U chorych z upośledzeniem czucia w zakresie ściany odbytnicy jako przyczyną NS stosuje się alternatywną formę treningu behawioralnego – trening sensoryczny. Powtarzane ćwiczenia z umieszczonym w bańce odbytnicy balonem napełnianym określoną, stopniowo modyfikowaną objętością pozwalają u ponad połowy tych chorych ograniczyć nasilenie objawów NS.
Elektrostymulacja przezodbytowa
Jeśli nie stwierdza się ubytków morfologicznych w zakresie
kompleksu zwieraczy, przy obniżonej wydolności skurczowej i upośledzonym unerwieniu obwodowym, wydolną
metodą terapii
jest przezodbytowa elektrostymulacja (ES).18 Metoda stosowana
jest albo w monoterapii (w systemie domowym lub ambulatoryjnym),
albo w ramach leczenia skojarzonego, jako uzupełnienie treningu behawioralnego.
Specjalnie skonstruowaną elektrodę umieszcza się w kanale odbytu.
Dobrany pod względem częstotliwości, natężenia i amplitudy impuls
przekazywany jest z podręcznego generatora do elektrody.
Stymulowane zwieracze podlegają skurczowi. Czas trwania
leczenia jest przewidziany na kilka do kilkunastu miesięcy.21
Operacyjne metody leczenia nietrzymania stolca
U około 20–30% chorych z objawami NS nie udaje się uzyskać poprawy mimo stosowania technik nieoperacyjnych. Według zaleceń IFFGD kwalifikują się oni do leczenia operacyjnego – zawsze po minimum 6-miesięcznym intensywnym leczeniu zachowawczym (tj. BF, ES).3 Typ i zakres postępowania chirurgicznego zależy od tego, czy przyczyną utraty kontroli defekacji jest wrodzony brak zwieraczy, nabyte ich uszkodzenie, uszkodzenie ich unerwienia czy też powstałe zmiany czynnościowe w zakresie odbytnicy i odbytu (wgłobienie, uchyłek odbytnicy [rectocele], wypadanie odbytnicy).22
Plastyczna rekonstrukcja zwieraczy
U chorych z przerwaną ciągłością zwieraczy, u których ubytek nie przekracza 1/3 obwodu i zachowane jest ich unerwienie, postępowaniem z wyboru jest rekonstrukcja zwieraczy. Stosowane jest proste zszycie zwieraczy koniec do końca, jak i modyfikacja typu plastyka na zakładkę (overlapping sphincter repair; ryc. 1). Wydaje się, że w przypadku okołoporodowego uszkodzenia zwieraczy przewagę mają zabiegi doraźne, wykonywane nie później niż 12 godzin po uszkodzeniu. Jak przekonują niektórzy autorzy, znamiennie lepsze wyniki uzyskano, gdy były one wykonywane przez chirurgów z doświadczeniem w chirurgii kolorektalnej. Do tego typu rekonstrukcji kwalifikują się także ubytki zwieracza (poniżej 1/3 obwodu) powstałe wskutek urazów jatrogennych, wypadków komunikacyjnych, gwałtu lub praktyk seksualnych.3,23 Proste zszycie zwieraczy (koniec do końca) ustępuje obecnie plastyce na zakładkę.

Ryc. 1. Okołoporodowe uszkodzenie zwieracza. Obraz śródoperacyjny:
kikuty zwieracza przygotowane do zespolenia, efektywność zabiegu monitorowana
śródoperacyjnie sondą manometryczną (materiał własny)
Zabieg wykonuje się u pacjenta w znieczuleniu ogólnym, w ułożeniu ginekologicznym, bez konieczności całkowitego oczyszczenia jelita grubego (płukanie). Cięciem łukowatym ponad brzegiem odbytu odsłania się brzegi uszkodzonego zwieracza wewnętrznego i zewnętrznego. Następnie po odpreparowaniu i uwolnieniu kikutów zwieraczy zszywa się je szwami niewchłanialnymi lub szwami o długim okresie utrzymywania napięcia w tkankach, zakładając wolne brzegi jeden na drugi – na zakładkę. W niektórych wypadkach zabieg połączony jest z plastyką ciała kroczowego (ryc. 2). Warunkiem powodzenia plastyki zwieraczy jest właściwa kwalifikacja chorych oraz doświadczenie chirurga wykonującego zabieg.
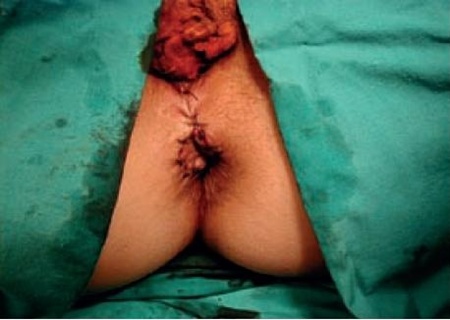
Ryc. 2. Stan po zabiegu plastyki zwieraczy na zakładkę i plastyce ciała kroczowego
Inne zabiegi rekonstrukcyjne
W 1975 roku Parks opisał technikę tylnej „naprawy” zwieraczy (postanal repair), która polega na zbliżeniu odnóg mięśnia łonowo-odbytniczego do tyłu od zwieraczy. Celem zabiegu jest przywrócenie zbliżonego do fizjologicznego kąta odbytniczo-odbytowego (anorectal angle), tym samym poprawa wydolności mechanizmu zaporowego kompleksu zwieraczy. Mimo że jeszcze kilka lat temu tylna plastyka była postępowaniem z wyboru, obecnie zabieg ten wykonuje się rzadko.24
Możliwości chirurgicznego leczenia krańcowego stadium nietrzymania stolca
Omówione w poprzednich podrozdziałach metody leczenia (BF, ES, proste zabiegi naprawcze) stanowią pierwszy etap leczenia NS. Jeżeli działania te nie przynoszą spodziewanych efektów, jeżeli nie uzyskano poprawy po prawidłowo przeprowadzonym leczeniu i rehabilitacji, należy rozważyć wykonanie zabiegów tak zwanych ratujących.
Transpozycja mięśni własnych (gluteoplastyka, gracyloplastyka)
Badania morfologiczne wykazały, że z dostępnych do transpozycji mięśni szkieletowych mięsień smukły uda najbardziej przypomina zwieracze odbytu właśnie pod względem budowy morfologicznej. Jak się jednak okazało w badaniach klinicznych, także ten mięsień nie potrafi utrzymać dłuższego skurczu, dlatego transpozycję mięśnia smukłego uzupełniono czasową stymulacją mięśnia wszczepioną elektrodą (tzw. gracyloplastyka dynamiczna) w celu przebudowy mięśnia z szybkokurczliwego, szybkomęczliwego (typ II) w mięsień wolnokurczliwy i wolnomęczliwy (typ I). Do powszechnego użycia weszły programowane zewnętrznie (przy użyciu fal radiowych) implantowane stymulatory firmy Medtronic o przedłużonej żywotności baterii (do lat 10;. ryc. 3). Wprawdzie koszty stymulatora, osprzętu i całego zabiegu są nadal duże (10–15 tys. dolarów), jednak efektywność takiego postępowania, a przede wszystkim całkowity powrót do pełnej aktywności społecznej i zawodowej chorych sprawia, że zyskuje ono znaczną popularność.25
Dynamiczną gracyloplastykę stosuje się także u chorych po brzuszno-kroczowym odjęciu odbytnicy z powodu nowotworu, jako element zabiegu całkowitej rekonstrukcji anorektalnej.
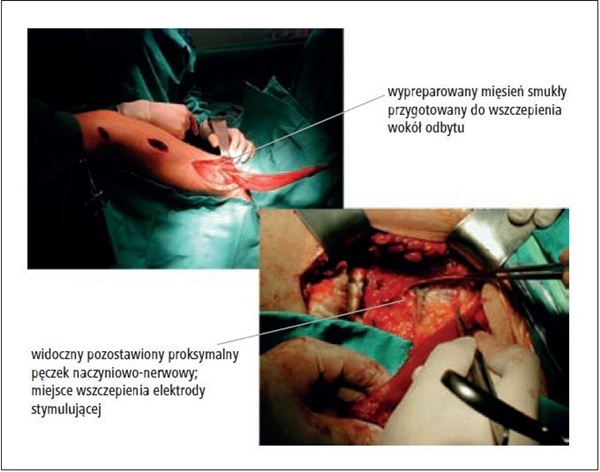
Ryc. 3. Zabieg gracyloplastyki (materiał własny)
Hydrauliczna proteza zwieracza jelitowego
Poza zwieraczami wytworzonymi z mięśni szkieletowych podobne zastosowanie w leczeniu NS znalazły zwieracze sztuczne (ryc. 4). Silikonowa proteza hydrauliczna jest implantowana na stałe i spełnia rolę mechanicznej zastawki. Poszczególne elementy stanowią zamknięty układ hydrauliczny wypełniony roztworem 1:1 zdemineralizowanej wody i środka kontrastowego, co pozwala na radiologiczną kontrolę położenia i sprawności układu po zabiegu (ryc. 5). Poprzez naciśnięcie aktywatora (balonik wypełniony płynem) wypełnia się mankiet umieszczony wokół ujścia odbytu, tym samym mechanicznie zamykając jego ujście. Przed defekacją poprzez nacisk na zaworek wypompowuje się z niego płyn do zbiornika wyrównującego, co umożliwia oddanie stolca.

Ryc. 4. Zestaw sztucznego zwieracza jelitowego:
1) zaworek umożliwiający otwarcie opaski; 2) opaska spełniająca
rolę mechanicznej zastawki; 3) aktywator, balonik umożliwiający napełnienie opaski płynem;
4) port kalibracyjny (materiał własny)
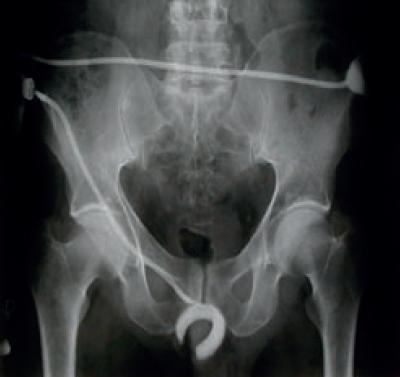
Ryc. 5. Radiogram pacjenta z wszczepionym układem sztucznego zwieracza (materiał
wlasny)
Transsakralna elektrostymulacja korzeni nerwów krzyżowych
Także inny typ leczenia NS zyskuje coraz większą popularność, zwłaszcza u chorych z uszkodzonym rdzeniem kręgowym, w przypadku których przyczyną NS nie jest uszkodzenie zwieraczy ani nerwu sromowego, a dróg nerwowych rdzenia. Zastosowanie trwałej transsakralnej elektrostymulacji (sacral nerve stymulation – SNS), przy użyciu odpowiednich elektrod implantowanych na stałe przez otwory kości krzyżowej połączonych z wszczepionym pod skórę stymulatorem sterowanym zewnętrznie (taki sam jak w dynamicznej gracyloplastyce), umożliwia uzyskanie częściowej, a w niektórych przypadkach nawet pełnej kontroli nad oddawaniem stolca. Doświadczenia Matzla i Rosena wskazują, że odpowiednia stymulacja korzonków S3, S4 pozwala na osiągnięcie zadowalających wyników czynnościowych u chorych z NS w wyniku uszkodzenia rdzenia. Metoda zdobywa coraz większe uznanie, a jej atrakcyjność zwiększa możliwość zminimalizowania urazu podczas implantacji elektrod.26
Nowe małoinwazyjne metody leczenia nietrzymania stolca
Procedura Secca®
Mimo że obecnie zabieg zwężania ujścia odbytu poprzez założenie przewiązki z drutu czy innego materiału obcego (zabieg Thierscha) jest już praktycznie historią, zasada, która legła u podstaw tego rodzaju interwencji zabiegowej, nie poszła w zapomnienie. Czasami jeszcze wykonywany w oryginalnej wersji zabieg ten stał się wzorem dla nowoczesnych technik operacyjnych. Przeprowadzony wokół zwieraczy drut powodował odczyn zapalny, a następnie zbliznowacenie. Obecnie podobny efekt, jednakże z możliwością kontroli jego zakresu, uzyskujemy poprzez działanie energii o wysokiej częstotliwości fal (radiofreguency energy – Secca® procedure). Postępowanie to określa się mianem remodelingu tkanki mięśniowej i włóknistej doprowadzającego do obkurczenia włókien kolagenu (blizny) i poprawy mechanicznej wydolności aparatu zaporowego zwieraczy. Dwuletnie obserwacje chorych poddanych tej procedurze pozwalają ocenić uzyskane wyniki leczenia jako znamienną poprawę kontroli defekacji i jakości życia. Modyfikację zabiegu Thierscha stanowią wszczepy opasek dakronowych pokrytych silikonem wokół odbytu. Zarówno jednak wyniki, jak i efekty uboczne tej metody leczenia nie budzą zachwytu.
Implantacja mikrobalonów i mikrosfer (Durasphere)
Implantację mikrobalonów stosowano już wcześniej w leczeniu nietrzymania moczu (stress incontinence). W przypadku NS zabieg polega na implantacji mikrobalonów w warstwę podśluzową kanału odbytu. Wykonuje się go w znieczuleniu dożylnym. Feretis i wsp. w 2001 roku opublikowali wyniki leczenia NS tą metodą. Uzyskali oni znamienną poprawę u wszystkich leczonych w ten sposób chorych. Nie zaobserwowali efektów ubocznych. Ze względu na małą grupę (6 chorych) metoda wymaga dalszych badań.27
Inny sposób polega na podawaniu środków zwiększających objętość masy tkankowej w miejscu ubytku – implantacji mikrosfer (Durasphere).28 W znieczuleniu miejscowym, po wprowadzeniu anoskopu, podaje się choremu środek zwiększający masę (objętość) – bulking agent (Durasphere) – w miejsce zlokalizowanego wcześniej ubytku zwieraczy. Według Davis i wsp. środek podaje się w postaci 1–4 iniekcji podśluzówkowych po 0,5–3 ml. Jest to małoinwazyjna, efektywna metoda leczenia NS u osób z widocznym ubytkiem zwieracza wewnętrznego. Wymaga jednak dalszych badań obejmujących większe grupy chorych. Podobne efekty uzyskuje się poprzez aplikację silikonu lub autologicznego tłuszczu.
Postępowanie „paliatywne”
Czasami wobec nieskuteczności lub braku możliwości leczenia konieczne jest wykonanie prostych zabiegów umożliwiających codzienne płukanie jelita u chorych pozbawionych całkowicie kontroli oddawania stolca (np. chorych neurologicznie), jak np. appendicostomia czy specjalna kolostomia (tzw. colonic conduit) zaproponowana przez Williamsa. W przypadku chorych, u których zawiodły wszystkie inne operacyjne sposoby leczenia, w ostateczności należy rozważyć wytworzenie sztucznego odbytu. W wybranych przypadkach zabieg ten może być postępowaniem z wyboru. Do takich chorych zalicza się pacjentów z demencją, z porażeniem kończyn dolnych i odleżynami.3
Podsumowanie
Wyniki leczenia NS niezależnie od stosowanych metod nie należą do rewelacyjnych. Odsetek bardzo dobrych i dobrych wyników po leczeniu zabiegowym, niezależnie od metody, wciąż nie przekracza 60%. Przedstawione metody wytworzenia zwieraczy zastępczych z własnych mięśni czy sztucznych zwieraczy są obarczone 80% ryzykiem powikłań, a konieczny do wykonania zabiegu osprzęt przekracza wciąż możliwości finansowe wielu chorych i ubezpieczycieli. Dlatego też pojawiają się nowe metody, w większości bazujące na opisanych przed laty wzorcach. Wszystkie one mają na celu osiągnięcie jak najlepszego wyniku leczenia przy stosunkowo niewielkim obciążeniu dla chorego, zarówno wynikającym z wykonania procedury jak i finansowym.
Należy mieć na uwadze, że ostatecznym celem leczenia pacjentów z dużego stopnia NS nie jest uzyskanie pełnej kontroli wypróżnień, w większości przypadków jest to bowiem niemożliwe. Podstawowym celem powinna być poprawa jakości życia, codziennej egzystencji, z możliwością prowadzenia aktywności w postaci wykonywania pracy i korzystania z życia towarzyskiego czy rozrywki w stopniu zaspokajającym potrzeby psychosocjalne pacjenta.
PIŚMIENNICTWO
1. Nelson R., Norton N., Cautley E., Furner S.: Community based prevalence of anal inconti1. nence. JAMA,
1995; 274: 559–561
2. Whitehead W.E., Wald A., Norton N.J.: Treatment options for fecal incontinence Dis. 2. Colon Rectum,
2001; 44: 131–144
3. Baeten C.G., Konsten J., Spaans F. i wsp.: Dynamic gracilloplasty for treatment of fecal incon3.
tinence. Lancet, 1991; 338: 1163–1165
4. American Medical Systema. Fecal incontinence scoring system. Minnetonca, American 4. Medical Systems
1997
5. Jorge J.M., Wexner S.D.: Etiology and management of fecal incontinence. Dis. Colon Rectum, 5. 1993;
36: 77–97
6. Pescatori M., Anastasio G., Bottini C., Mentasti A.: New grading and scoring for anal incon6.
tinence: evaluation of 335 patients. Dis. Colon Rectum, 1992; 35: 482–487
7. Feldman M., Schiller L.R.: Disorders of gastrointestinal motility associated with diabetes 7.
mellitus. Ann. Int. Med., 1983; 98: 378–384
8. Herman R.M., Wałęga P., Herman K. i wsp.: Low anterior resection syndrome – clinical 8.
manometric and videoproctographic evaluation 2 years after surgery. Monduzzi Editore Proceedings of The
Eurosurgery, 2002; 265–270
9. Wałega P., Herman R.M., Popiela T.: Odległe wyniki oceny funkcji zwieraczy u chorych 9. po
przedniej niskiej resekcji odbytnicy. Pol. Przegl. Chir., 2001; 73: 327–245
10. Damon H., Henry L.,Barth X., Mion F.: Fecal incontinence in females with a past history 10. of
vaginal delivery: significance of anal sphincter defects detected by ultrasound. Dis. Colon Rectum, 2002;
45: 1445–1450
11. de Parades V., Etienney I., Thabut D. i wsp.: Anal sphincter injury after forceps delivery: 11.
myth or reality? A prospective ultrasound study of 93 females. Dis. Colon Rectum, 2004; 47: 24–34
12.Hinds J.P., Eidelam B.H.,Wald A.: Prevalence of bowel dysfunction in multiple sclerosis. 12. A population
survey. Gastroenterology, 1990; 98: 1538–1542
13. Stelzner F.: Über die Anatomie des analen Sphincterorgans – wie der Chirurg sie sieht. Z. Anat. 13.
Entwick. Gesch., 1969; 121: 525–530
14. Hill J., Hosker G., Kiff E.S.: Pudendal nerve terminal motor latency measurements: what they 14. do
and do not tell us. Br. J. Surg., 2002; 89: 1268–1269
15. Herman R.M., Wałęga P., Widera A.: Biofeedback jako zachowawcza metoda leczenia nietrzy15. mania
stolca. Pol. Przegl. Lek., 2004; 1
16. Carpeti E.A., Kamm M.A., Philips R.K.S.: Randomized
controlled trial of topical phenyleph16. rine in treatment of fecal incontinence (Randomized Clinical
Trial). Br. J. Surg., 2000; 87: 38–41
17. McLeod J.H.: Biofeedback in treatment of partial anal incontinence. Dis. Colon Rectum,1983; 26:
244–246
18. Herman R.M., Wałega P., Nowakowski M. i wsp.: Transanal electrostimulation in the treat18. ment
of fecal incontinence following low anterior rectum resection. International Proceedings Division. Monduzzi
Editore, 2001; 295–299
19. Norton C., Hoscer G., Brazzelli M.: Biofeedback and/or sphincter exercises for the treat19. ment of
faecal incontinence in adults (Cochrane review). Cochrane Library, Oxford Update Software 2000; Issue
3
20.
Vaizey C.J., Kamm M.A., Nicholls R.J.: Recent advances in the surgical treatment of faecal 20. incontinence.
Br. J. Surg., 1998; 85; 596–603
21. Malouf A.J. Vaizey C.J., Kamm M.,Nichols R.J.: Reassessing artificial bowel sphincters. Lancet, 21.
2000; 355: 2219–2200
22. Oliveira R., Pfeifer J., Wexner S.D.: Physiological and clinical outcome of anterior sphinc22.
teroplasty. Br. J. Surg., 1996; 83: 502–505
23. Tighe M., Taylor B.A.: Emergency repair of obstetric injury to the anal sphincters – a role 23.
for the colorectal surgeon. Triplate 2002 colorectal meeting abstracts. Dis. Colon Rectum, 2002; 45: abstr.
35
24. Athanasiadis S., Sanchez M., Nafe M.: Ergebnisse der anterioren Levator und Externusplastik 24. bei
der idiopatischen anorectalen Incontinenz. Chirurg, 1994; 65: 634–641
25. Herman R.M., Wałega P., Nowakowski M. i wsp.: Dynamic gracilloplasty in Poland. 25.
Proktologia, 2001; 2: 179–185
26. Ratto C., Morelli U., Paparo S. i wsp.: Minimall invasive sacral neuromodulation implant 26.
technique: modifications to the conventional procedure. Dis. Colon Rectum, 2003; 46: 414–417
27. Feretis C., Benakis P., Dailianas A. i wsp.: Implantation of microballoons in the management
27. of fecal incontinence. Dis. Colon Rectum, 2001; 44: 1605–1609
28. Devis K., Kumar D.: Clinical evaluation of injectable anal sphincter bulking agent (Durasphere) 28.
in management of patients with persistent faecal incontinence secondary to internal anal sphincter defect.
Dis. Colon Rectum, 2002; 45